- Autor Rachel Wainwright wainwright@abchealthonline.com.
- Public 2023-12-15 07:39.
- Zuletzt bearbeitet 2025-11-02 20:14.
Magnevist
Magnevist: Gebrauchsanweisung und Bewertungen
- 1. Form und Zusammensetzung freigeben
- 2. Pharmakologische Eigenschaften
- 3. Anwendungshinweise
- 4. Gegenanzeigen
- 5. Art der Anwendung und Dosierung
- 6. Nebenwirkungen
- 7. Überdosierung
- 8. Besondere Anweisungen
- 9. Anwendung während der Schwangerschaft und Stillzeit
- 10. Verwendung in der Kindheit
- 11. Bei eingeschränkter Nierenfunktion
- 12. Wechselwirkungen mit anderen Medikamenten
- 13. Analoge
- 14. Lagerbedingungen
- 15. Bedingungen für die Abgabe an Apotheken
- 16. Bewertungen
- 17. Preis in Apotheken
Lateinischer Name: Magnevist
ATX-Code: V08CA01
Wirkstoff: Gadopentetinsäure (Gadopentetinsäure)
Hersteller: Bayer Pharma, AG (Bayer Pharma, AG) (Deutschland); Werk Medsintez (Russland)
Beschreibung und Foto-Update: 27.11.2008
Magnevist ist ein Kontrastdiagnosewerkzeug für die Magnetresonanztomographie (MRT).
Form und Zusammensetzung freigeben
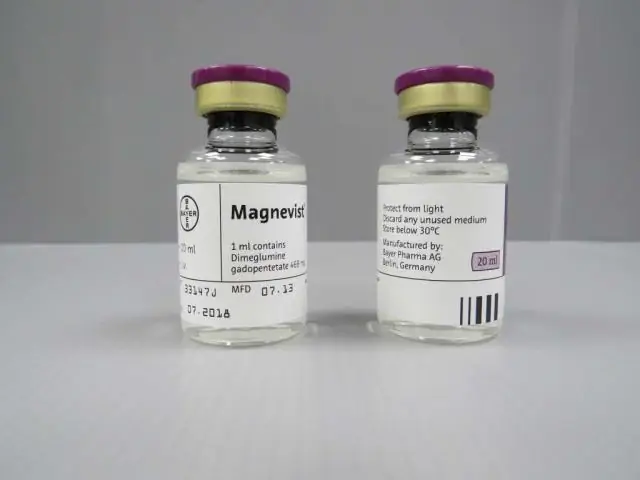
Magnevist wird in Form einer Lösung zur intravenösen (iv) Verabreichung hergestellt: eine klare, farblose oder fast farblose Flüssigkeit, frei von Fremdpartikeln (jeweils 5, 10, 15, 20 oder 30 ml) in einem Glasfläschchen der hydrolytischen Klasse I, verschlossen mit einem Gummistopfen und gerollt in einer Aluminiumkappe; 10, 15 oder 20 ml in einer Plastik- oder Glasspritze, 1 Spritze in einem versiegelten PVC-Behälter; in einem Karton 1, 5 oder 10 Flaschen / Behälter und Gebrauchsanweisung von Magnevist).
1 ml einer wässrigen Lösung enthält:
- Wirkstoff: Dimegluminsalz der Gadopentetinsäure - 469,01 mg, was Gadopentetat-Dimeglumin in einer Menge von 0,5 mmol entspricht [Osmolalität der Substanz (Osm / kg H 2 O) bei 37 ° C beträgt 1,96; Viskosität (mPa s) bei 20 ° C - 4,9, bei 37 ° C - 2,9; Dichte (g / ml) bei 20 ° C - 1,21, bei 37 ° C - 1,195; pH - 7-7,9];
- zusätzliche Komponenten: Pentessinsäure (Diethylentriaminpentaessigsäure - DTPA), Meglumin, Wasser zur Injektion.
Pharmakologische Eigenschaften
Pharmakodynamik
Magnevist ist ein paramagnetisches Kontrastmittel für die MRT. Der kontrastierende Effekt, den es zeigt, beruht auf dem Di-N-methylglucaminsalz von Gadopentetat, einem Komplex von Gadolinium mit DTPA. Bei Verwendung der geeigneten Abtastsequenz (z. B. der T 1 -gewichteten Spin-Echo- Methode) für die Protonen-Magnetresonanztomographie verkürzen Gadoliniumionen die Spin-Gitter-Relaxationszeit der Atomkerne im Anregungszustand, was zu einer Erhöhung der Signalintensität und einer Erhöhung des Bildkontrasts führt bestimmte Gewebe.
Dimeglumin-Gadopentetat neigt nicht zur Bindung an Proteine und hemmt nicht die Enzymaktivität (einschließlich myokardialer Na + -K + -ATPase). Magnevist aktiviert das Komplementsystem nicht und hat daher ein sehr geringes Potenzial, die Entwicklung anaphylaktoider Reaktionen zu induzieren.
Pharmakokinetik
Dimeglumin-Gadopentetat ist eine Verbindung mit ausgeprägten paramagnetischen Eigenschaften, die die Relaxationszeit selbst bei Verwendung in geringen Konzentrationen erheblich verkürzt.
Die Pharmakokinetik des Wirkstoffs ähnelt der Pharmakokinetik anderer biologisch inerter Verbindungen mit hoher Hydrophilie (einschließlich Inulin oder Mannit) und hängt nicht von seiner Dosis ab. Nach intravenöser Verabreichung ist das Mittel schnell genug im extrazellulären Raum verteilt. Wenn Gadopentetat-Dimeglumin in Dosen unter 0,25 mmol / kg Körpergewicht (entspricht Magnevist in einer Dosis von 0,5 ml / kg) angewendet wird, nimmt nach einer mehrminütigen schnellen Verteilungsphase die Blutkonzentration ab, die Halbwertszeit (T 1/2)) beträgt ca. 90 Minuten. Nach der Einführung des Wirkstoffs in einer Dosis von 0,1 mmol / kg (entspricht Magnevist in einer Dosis von 0,2 ml / kg) nach 3 und 60 Minuten beträgt sein Plasmaspiegel im Blut 0,6 bzw. 0,24 mmol.
Das Medikament überschreitet nicht die Blut-Hoden-Schranke oder die intakte Blut-Hirn-Schranke (BBB). in geringer Menge dringt in die Plazentaschranke ein und wird schnell vom Fötus ausgeschieden.
Der Wirkstoff wird mittels glomerulärer Filtration unverändert über die Nieren ausgeschieden, nur ein kleiner Teil des Arzneimittels wird einer extrarenalen Ausscheidung ausgesetzt. Im Durchschnitt werden nach der Injektion nach 6 und 24 Stunden 83 bzw. 91% der verabreichten Dosis eliminiert, weniger als 1% werden innerhalb von 5 Tagen über den Darm ausgeschieden. Bei einer Körperoberfläche von 1,73 m 2 beträgt die renale Clearance von Gadopentetat-Dimeglumin ungefähr 120 ml / min.
Anwendungshinweise
Magnevist wird für die MRT des Gehirns und des Rückenmarks (kraniale und spinale MRT) verwendet, um den Bildkontrast in den folgenden Studien zu verbessern:
- Differentialdiagnose bei Verdacht auf Hörnervenneurom, Meningiom, Tumoren mit infiltrativem Wachstum in nahegelegene Gewebe (z. B. Gliom);
- Erkennung von Tumoren, einschließlich kleiner und schlecht sichtbarer Tumoren, Tumorrezidiv nach Operation oder Strahlentherapie, Metastasen;
- Differentialdiagnose einiger seltener Tumoren (Ependymom, Hämangioblastom, kleine Hypophysenadenome);
- verbesserte Visualisierung der intrakraniellen Ausbreitung von extrazerebralen Tumoren.
Zusätzliche Indikationen für die Anwendung von Magnevist während der spinalen MRT:
- Differentialdiagnose von extramedullären und intramedullären Tumoren;
- Einschätzung der Prävalenz von intramedullären Tumoren;
- Feststellung der Größe solider Tumoren im Rückenmark.
Bei der MRT des gesamten Körpers (einschließlich der Untersuchung des Halsbereichs, des Gesichtsbereichs des Schädels, der Brustdrüsen bei Frauen, der Brust- und Bauchhöhlen, der Beckenorgane, des Bewegungsapparates, um ein Bild der Gefäße des gesamten Körpers zu erhalten) zur Verbesserung des Bildkontrasts wird Magnevist verwendet für folgende Zwecke:
- Identifizierung und / oder Feststellung der Prävalenz und der Grenzen des Entzündungsprozesses, des Tumors, der Gefäßschädigung;
- Differentialdiagnose von Tumoren und Narbengewebe nach der Therapie;
- Beurteilung der Blutversorgung normaler und pathologisch veränderter Gewebe;
- Differentialdiagnose der Struktur pathologischer Veränderungen;
- Identifizierung des Wiederauftretens eines Bandscheibenvorfalls nach der Operation;
- gleichzeitige semi-quantitative Beurteilung der Nierenfunktion und deren Visualisierung.
Kontraindikationen
Das Medikament ist für die Anwendung bei bestehender Überempfindlichkeit gegen seine Bestandteile kontraindiziert.
Ein Kontrastmittel sollte unter folgenden Bedingungen / Krankheiten mit äußerster Vorsicht angewendet werden:
- Epilepsie;
- schweres Kreislaufversagen;
- Bronchialasthma;
- eine Vorgeschichte von allergischen Reaktionen;
- Schwangerschaft;
- schwere Nierenfunktionsstörung mit Kreatinin-Clearance (CC) unter 20 ml / min.
Magnevist, Gebrauchsanweisung: Methode und Dosierung
Magnevist ist ausschließlich zur intravenösen Verabreichung bestimmt. Unmittelbar nach der Injektion des Arzneimittels können Sie eine MRT-Studie mit Kontrastmittel starten. Der Agent wird nicht zur Verabreichung unter den Meningen verwendet.
Im Bereich von 0,14 bis 1,5 T hängen die empfohlenen Dosen des Arzneimittels nicht von der Stärke des Magnetfelds ab.
Es ist erforderlich, Magnevist aus einer Durchstechflasche in eine Spritze zu sammeln oder eine Fertigspritze aus einem verschlossenen Behälter herauszunehmen und unmittelbar vor der Verabreichung von einer Schutzkappe zu lösen. Der Gummistopfen der Flasche darf nicht mehr als einmal mit der Lösung durchstoßen werden. Die Reste des Kontrastmittels, die während der Untersuchung nicht verwendet wurden, müssen entsorgt werden.
Es wird empfohlen, einen flexiblen Katheter oder eine Kanüle zur intravenösen Verabreichung der Lösung zu verwenden. Es ist erforderlich, das Medikament nur in einem Krankenhaus mit Geräten zu verwenden, die für die Notfallversorgung in Notsituationen ausgelegt sind, einschließlich der Durchführung von Wiederbelebungsmaßnahmen. Während der MRT müssen die üblichen Vorsichtsmaßnahmen für diese Methode beachtet werden (Patienten dürfen keine Herzschrittmacher, Gefäßklammern aus ferromagnetischen Materialien usw. haben).
Während der intravenösen Verabreichung der Lösung sollte sich der Patient (wenn möglich) in horizontaler Position befinden und nach der Injektion mindestens 30 Minuten lang unter strenger ärztlicher Aufsicht stehen.
Bei Kindern über 2 Jahren und Erwachsenen kann die intravenöse Verabreichung des Arzneimittels manuell oder unter Verwendung eines automatischen Injektors erfolgen. Bei Kindern unter 2 Jahren, einschließlich Neugeborenen (bis zu 1 Monat), muss die Lösung ausschließlich von Hand verabreicht werden.
Bei Patienten mit mäßiger Nierenschädigung (CC beträgt 30-60 ml / min) und Kindern im Alter von 1 bis 12 Monaten sollte die Anwendung des Arzneimittels auf die Einführung einer Standarddosis (0,1 mmol / kg) beschränkt sein, während eine wiederholte Verabreichung nicht früher erfolgen kann als 7 Tage später.
Für Studien mit Kontrastverstärkung beim Scannen werden in der Regel T 1 -gewichtete Sequenzen verwendet.
Empfohlenes Dosierungsschema:
- kraniale und spinale MRT: Kindern (einschließlich Neugeborenen und Säuglingen), Jugendlichen und Erwachsenen wird 0,2 ml / kg injiziert; Wenn nach der Studie der Verdacht auf das Vorhandensein einer Läsion besteht, kann für eine genauere Diagnose eine zweite Kontraststudie durchgeführt werden. 30 Minuten nach der ersten Injektion des Arzneimittels wird die Dosis erneut mit einer Dosis von 0,2 / 0,4 ml / kg injiziert, gefolgt von einer sofortigen MRT.
- Ganzkörper-MRT: Erwachsene und Kinder über 2 Jahre werden mit 0,2 ml / kg injiziert, wenn sich die Läsion in einem Bereich mit geringem Vaskularisierungsgrad und / oder mit einem unbedeutenden extrazellulären Raum befindet. Um einen angemessenen Kontrasteffekt zu erzielen, kann es erforderlich sein, ein Arzneimittel in einer Dosis von 0 zu verabreichen. 4 ml / kg, insbesondere bei Verwendung kurzer T 1 -gewichteter Sequenzen beim Scannen.
Die Einführung von Magnevist in einer Dosis von 0,6 ml / kg bei erwachsenen Patienten kann die Zuverlässigkeit der Diagnose bei vielen pathologischen Läsionen oder wiederkehrenden Tumoren erhöhen. Für Erwachsene beträgt die maximale Einzeldosis 0,6 ml / kg, für Kinder 0,4 ml / kg.
Zur Visualisierung der Gefäße kann Erwachsenen je nach Untersuchungsort und angewandter MRT-Technik eine maximale Einzeldosis von 0,6 ml / kg verschrieben werden.
Nebenwirkungen
- Herz-Kreislauf-System: selten - Blutdruckabfall, Ohnmacht, Zyanose, periphere Vasodilatation, Reflextachykardie, arterielle Hypotonie, Arrhythmie, Herzstillstand;
- Nervensystem: manchmal - Kopfschmerzen, Schwindel, Parästhesien; selten - Schläfrigkeit, Asthenie, Zittern, Unruhe, Unruhe, Sprachstörungen, Krämpfe, Koma;
- Verdauungssystem: manchmal - Erbrechen, Übelkeit; selten - Hypersalivation, Mundtrockenheit, Geschmacksperversion, Bauchschmerzen, Durchfall, erhöhte Aktivität von Bilirubin und Leberenzymen im Blut (vorübergehend);
- Sinnesorgane: selten - Schmerzen in den Ohren, Schmerzen in den Augen, tränende Augen, Seh- / Hör- / Geruchsstörungen;
- Atmungssystem: selten - Husten, Atemnot, Lungenödem, Atemversagen, Atemstillstand;
- dermatologische Reaktionen: selten - Juckreiz, Hautausschlag, Hautrötung (aufgrund von Vasodilatation), Ödeme;
- Harnsystem: selten - häufiger Harndrang, Harninkontinenz; bei Patienten mit früheren Nierenschäden - eine Erhöhung der Kreatininkonzentration im Blut und akutes Nierenversagen;
- allergische Reaktionen: selten - Hautreaktionen (Urtikaria), Bindehautentzündung, Niesen, Rhinitis, Husten, Bronchospasmus, Laryngospasmus, Kehlkopf- / Rachenödem, Angioödem, arterielle Hypotonie, Schock;
- lokale Reaktionen: selten im Falle einer Extravasation - ein Gefühl von Wärme / Kälte, Entzündung, lokalen Schmerzen, Ödemen, Venenentzündung, Thrombophlebitis, Gewebenekrose;
- allgemeine Reaktionen: manchmal - Kopfschmerzen, Hitzegefühl; selten - vermehrtes Schwitzen, Unwohlsein, Brust- / Gelenkschmerzen, Rückenschmerzen, Fieber, Ohnmacht;
- andere: selten - ein vorübergehender Anstieg des Eisenspiegels im Blutserum.
Überdosis
Symptome einer Überdosierung von Gadopentetinsäure können Manifestationen von Hyperosmotizität sein - Druckanstieg in der Lungenarterie, Hypervolämie, erhöhter Urinausstoß, Dehydration.
Dieser Zustand erfordert die Überwachung der Nierenfunktion, insbesondere bei Patienten mit Nierenversagen. Dimeglumin-Gadopentetat wird durch Hämodialyse aus dem Körper ausgeschieden.
spezielle Anweisungen
Der Patient sollte zwei Stunden vor der Untersuchung auf das Essen verzichten, um das Aspirationsrisiko zu verringern.
Die Einführung von Gadopentetinsäure kann zu schwerwiegenden allergischen Reaktionen (einschließlich anaphylaktischem Schock) führen, von denen die meisten innerhalb von 30 Minuten nach der Injektion auftreten. In einigen Fällen können sich jedoch verzögerte Reaktionen entwickeln, die mehrere Stunden oder Tage nach der Studie auftreten.
Vor der Verschreibung des Arzneimittels muss eine allergische Anamnese von Patienten auf Asthma bronchiale, Urtikaria, Heuschnupfen, allergische Reaktionen auf Meeresfrüchte und Empfindlichkeit gegenüber Kontrastmitteln sorgfältig erfasst werden. Patienten aus dieser Risikogruppe wird empfohlen, eine Prämedikation mit Blockern von Histamin-H1-Rezeptoren und / oder Glukokortikoiden (GCS) durchzuführen.
Bei Patienten mit Asthma bronchiale wird während der Anwendung von Magnevist die Gefahr von Bronchospasmus oder Überempfindlichkeitsreaktionen verstärkt.
Bei Patienten mit intrakraniellen Tumoren oder Metastasen und mit Epilepsie in der Vorgeschichte steigt das Risiko häufigerer Anfälle nach Verabreichung von Kontrastmitteln.
Wenn der Eisenspiegel im Blutserum während der ersten 24 Stunden durch komplexometrische Methoden (z. B. mit Hilfe von Batophenanthrolin) ermittelt wird, kann der quantitative Indikator aufgrund des Vorhandenseins eines Kontrastmittels DTPK in der Lösung verringert werden.
Einfluss auf die Fahrfähigkeit von Fahrzeugen und komplexe Mechanismen
Es wurde kein negativer Effekt von Gadopentetinsäure auf die Fähigkeit, Fahrzeuge zu fahren und andere komplexe Geräte zu kontrollieren, gefunden.
Anwendung während der Schwangerschaft und Stillzeit
Die Sicherheit der Anwendung von Magnevist während der Schwangerschaft wurde nicht untersucht. Wenn die Lösung schwangeren Frauen verabreicht werden muss, ist besondere Vorsicht geboten.
Das Medikament kommt in sehr geringen Mengen in der Muttermilch vor - nicht mehr als 0,04% der verwendeten Dosis. Die verfügbaren Daten zeigen, dass durch die Einführung von Kontrastmitteln bei Müttern keine Gefahr für die Gesundheit gestillter Kinder besteht.
Verwendung im Kindesalter
Die Erfahrungen mit der Verwendung einer Kontrastmittellösung für die Ganzkörper-MRT bei Kindern unter 2 Jahren sind derzeit begrenzt. Vor der Durchführung von Studien mit Magnevist bei Patienten dieser Altersgruppe muss das Verhältnis des erwarteten Nutzens und des möglichen Risikos für die Entwicklung negativer Nebenwirkungen sorgfältig abgewogen werden.
Mit eingeschränkter Nierenfunktion
Bei mittelschwerer und leichter Nierenfunktionsstörung (CC über 20 ml / min) wird Dimeglumin-Gadopentetat fast vollständig über die Nieren ausgeschieden. T 1/2 im Plasma steigt proportional zum Grad der Funktionsstörung der Nieren an, aber es gibt keine Zunahme der extrarenalen Ausscheidung.
Bei schwerem Nierenversagen (CC unter 20 ml / min) muss vor der Anwendung des Arzneimittels eine gründliche Bewertung des beabsichtigten Nutzens und des potenziellen Risikos seiner Verabreichung durchgeführt werden, da sich die Ausscheidung des Kontrastmittels in diesem Fall verzögern kann. Wenn bei dieser Patientengruppe T 1/2 30 Stunden nicht erreicht, kann das Arzneimittel durch extrakorporale Hämodialyse aus dem Körper entfernt werden.
Wechselwirkungen mit anderen Medikamenten
Bei Verwendung von Kontrastmitteln vor dem Hintergrund einer Therapie mit β-Blockern kann es zu einer Zunahme von Überempfindlichkeitsreaktionen kommen.
Wechselwirkungen von Dimeglumin-Gadopentetat mit anderen Arzneimitteln / Wirkstoffen wurden nicht nachgewiesen.
Analoge
Magnevists Analoga sind Gadopentetinsäure-TL, Multichane, Omniscan, Gadovist, Magnilek, Tomovist, OptiMARK, Gadodiamid.
Lagerbedingungen
Darf nicht in die Hände von Kindern gelangen und vor Licht geschützt werden.
Die Haltbarkeit des Arzneimittels in Glasfläschchen und Spritzen beträgt 5 Jahre, in Plastikspritzen 3 Jahre.
Abgabebedingungen von Apotheken
Verschreibungspflichtig.
Bewertungen über Magnevist
Es gibt nur sehr wenige Bewertungen über Magnevist und sie sind normalerweise positiv. Experten stellen fest, dass sich das Kontrastmittel für die MRT bei der Diagnose von Gefäßerkrankungen, onkologischen Läsionen des Gehirns und des Rückenmarks sowie bei der MRT des gesamten Körpers bewährt hat. Gleichzeitig empfehlen sie, Patienten, die anfällig für Allergien oder schwere Nierenfunktionsstörungen sind, besondere Sorgfalt zu erweisen.
Patienten während der Anwendung des Arzneimittels bemerkten keine schwerwiegenden Komplikationen, während der Diagnose gab es keine Beschwerden und die Nebenwirkungen waren entweder nicht vorhanden oder hatten einen milden Charakter.
Der Preis von Magnevist in Apotheken
Der Preis für Magnevist (Lösung zur intravenösen Verabreichung von 0,5 mmol / ml) beträgt im Durchschnitt: für eine Packung mit 10 Durchstechflaschen mit 15 ml - 25.000 Rubel, für eine Packung mit 10 Durchstechflaschen mit 20 ml - 34.000 Rubel. für eine Packung mit 10 Glasspritzen von 15 ml - 27.000 Rubel.

Maria Kulkes Medizinjournalistin Über den Autor
Ausbildung: Erste Moskauer Staatliche Medizinische Universität nach I. M. Sechenov, Fachgebiet "Allgemeinmedizin".
Informationen über das Medikament werden verallgemeinert, nur zu Informationszwecken bereitgestellt und ersetzen nicht die offiziellen Anweisungen. Selbstmedikation ist gesundheitsschädlich!